Unlike conventional mRNA պատվաստանյութեր which encodes only for the target antigens, the self-amplifying mRNAs (saRNAs) encodes for non-structural proteins and promotor as well which makes saRNAs replicons capable of transcribing in vivo in the host cells. Early results indicates that their effectiveness, when given in smaller doses, is at par with that of regular doses of conventional mRNA. Due to low dose requirements, fewer side effects and longer duration of action, saRNA appears as better RNA platform for vaccines (including for v.2.0 of mRNA COVID vaccines) and newer therapeutics. No saRNA-based vaccine or drug is approved for human use yet. However, significant progress in this area has the potential to usher in a renaissance in prevention and treatment of infections and degenerative disorders.
Needless to say, mankind is frail before pandemics like COVID. We all experienced it and were impacted by it in one way or other; millions could not live to see the next morning. Given China too had massive COVID-19 immunisations programme, the latest media reports of spurts of cases and mortality in and around Beijing is concerning. The need of preparedness and relentless pursuit of more effective պատվաստանյութեր and therapeutics cannot be underemphasised.
The extraordinary situation presented by the COVID-19 pandemic provided an opportunity for the promising RNA technology to come out of age. Clinical trials could be completed at a record pace and mRNA based COVID Պատվեր, BNT162b2 (manufactured by Pfizer/BioNTech) and mRNA-1273 (by Moderna) received EUA from the regulators and, in due course, played an important role in providing protection against the pandemic to the people especially in Europe and North America1. These mRNA պատվաստանյութեր are based on synthetic RNA platforms. This allows for rapid, scalable and cell-free industrial production. But these are not without limitations such as high cost, cold supply chain, diminishing antibody titres, to name a few.
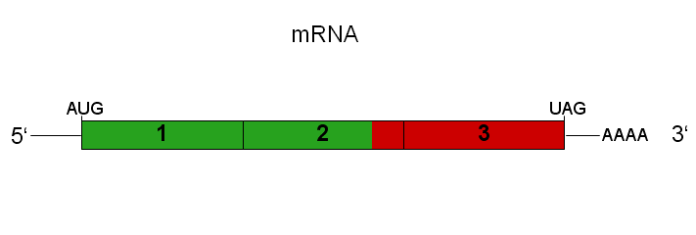
mRNA պատվաստանյութեր currently in use (sometimes referred to as conventional or 1st generation mRNA պատվաստանյութեր) are based on encoding the viral antigen in synthetic RNA. A non-viral delivery system transports the transcript to the host cell cytoplasm where the viral antigen is expressed. The expressed antigen then induces immune response and provide active immunity. Because RNA degrades easily and this mRNA in the vaccine cannot self-transcribe, an appreciable amount of synthetic viral RNA transcripts (mRNA) need to be administered in the vaccine for eliciting desired immune response. But what if the synthetic RNA transcript is incorporated also with non-structural proteins and promotor genes, in addition to the desired viral antigen? Such an RNA transcript will have ability to transcribe or self-amplify itself when transported into the host cell though it will be longer and heavier and its transport to the host cells may be more complex.
Unlike conventional (or, non-amplifying) mRNA which has codes only for the targeted viral antigen, the self-amplifying mRNA (saRNA), has ability to transcribe itself when in vivo in the host cells by virtue of presence of required codes for non-structural proteins and a promotor. mRNA vaccine candidates based on self-amplifying mRNAs are referred to as second or next generation mRNA պատվաստանյութեր. These offer better opportunities in terms of lower dosage requirements, relatively fewer side effects, and longer duration of action/effects (2-5). Both the versions of RNA platform are known to the scientific community for some time. In pandemic response, researchers opted for non-replicating version of mRNA platform for vaccine development in view of its simplicity and exigencies of pandemic situation and to gain experience with non-amplifying version first as prudence warranted. Now, we have two approved mRNA պատվաստանյութեր against COVID-19, and several vaccine and therapeutics candidates in pipeline such as ՄԻԱՎ-ի պատվաստանյութ և բուժում Charcot-Marie-Tooth հիվանդություն.
SARNA պատվաստանյութի թեկնածուները COVID-19-ի դեմ
SaRNA պատվաստանյութի նկատմամբ հետաքրքրությունն այնքան էլ նոր չէ։ Համաճարակի սկզբից մի քանի ամսվա ընթացքում՝ 2020 թվականի կեսերին, Մակքեյը et al. ներկայացրել է saRNA-ի վրա հիմնված պատվաստանյութի թեկնածու, որը ցույց է տվել մկների շիճուկներում հակամարմինների բարձր տիտր և վիրուսի լավ չեզոքացում։6. The phase-1 clinical trial of VLPCOV–01 (a self-amplifying RNA vaccine candidate) on 92 healthy adults whose results were published on preprint last month concluded that low dose administration of this saRNA based vaccine candidate induced immune response comparable to conventional mRNA vaccine BNT162b2 and recommends its further development as booster vaccine7. In another recently published study conducted as part of the COVAC1 clinical trial to develop booster dose administration strategy, a superior immune response was found in people who had previous COVID-19 and received a novel self-amplifying RNA (saRNA) COVID-19 vaccine plus a UK authorised vaccine8. A pre-clinical trial of novel oral vaccine candidate based on self-amplifying RNA on mouse model elicited high antibody titre9.
Գրիպի դեմ saRNA պատվաստանյութի թեկնածու
Influenza պատվաստանյութեր currently in use are based on inactivated viruses or synthetic recombinant (synthetic HA gene combined with a baculovirus)10. A self-amplifying mRNA-based vaccine candidate may induce immunity against multiple viral antigens. Pre-clinical trial of sa-mRNA bicistronic A/H5N1 vaccine candidate against influenza on mice and ferrets elicited potent antibody and T-cell response warranting evaluation on humans in clinical trials11.
COVID-19-ի դեմ պատվաստանյութերը ակնհայտ պատճառներով ուշադրության են արժանացել։ Որոշ նախակլինիկական աշխատանքներ են կատարվել ՌՆԹ հարթակների կիրառման ուղղությամբ այլ վարակների և ոչ վարակիչ խանգարումների դեպքում, ինչպիսիք են քաղցկեղը, Ալցհեյմերի հիվանդությունը և ժառանգական խանգարումները. Այնուամենայնիվ, դեռևս ոչ մի saRNA-ի վրա հիմնված պատվաստանյութ կամ դեղամիջոց չի հաստատվել մարդկանց օգտագործման համար: Լրացուցիչ հետազոտություններ պետք է կատարվեն saRNA-ի վրա հիմնված պատվաստանյութերի օգտագործման վերաբերյալ՝ համակողմանիորեն հասկանալու համար դրանց անվտանգությունն ու արդյունավետությունը մարդկանց վրա օգտագործելու համար:
***
Հիշատակում:
- Prasad U., 2020. COVID-19 mRNA պատվաստանյութ. գիտության մեջ կարևոր իրադարձություն և բժշկության մեջ խաղի փոփոխություն: Գիտական եվրոպ. Հրատարակված է 29 թվականի դեկտեմբերի 2020-ին։ Հասանելի է առցանց՝ հասցեով http://scientificeuropean.co.uk/medicine/covid-19-mrna-vaccine-a-milestone-in-science-and-a-game-changer-in-medicine/
- Bloom, K., van den Berg, F. & Arbuthnot, P. Ինֆեկցիոն հիվանդությունների համար ինքնաուժեղացող ՌՆԹ պատվաստանյութեր: Theին Թեր 28, 117–129 (2021): https://doi.org/10.1038/s41434-020-00204-y
- Պուրսեյֆ Մ.Մ et al 2022. Ինքնահաստատվող mRNA պատվաստանյութեր. Գործողության եղանակ, նախագծում, մշակում և օպտիմալացում: Թմրամիջոցների հայտնաբերումն այսօր. Volume 27, Issue 11, November 2022, 103341. DOI: https://doi.org/10.1016/j.drudis.2022.103341
- Բլաքնի Ա.Կ et al 2021. An Update on Self-Amplifying mRNA Vaccine Development. Պատվաստանյութեր 2021, 9 (2), 97; https://doi.org/10.3390/vaccines9020097
- Աննա Բլաքնի; ՌՆԹ-ի հաջորդ սերնդի պատվաստանյութերը՝ ինքնաուժեղացող ՌՆԹ: Biochem (Լոնդ) 13 օգոստոսի 2021 թ. 43 (4): 14–17. doi: https://doi.org/10.1042/bio_2021_142
- McKay, PF, Hu, K., Blakney, AK et al. Ինքնահաստատվող ՌՆԹ SARS-CoV-2 լիպիդային նանոմասնիկների պատվաստանյութի թեկնածուն մկների մոտ առաջացնում է չեզոքացնող հակամարմինների բարձր տիտր: Nat Commun 11, 3523 (2020): https://doi.org/10.1038/s41467-020-17409-9
- Akahata W., et al 2022. SARS-CoV-2 ինքնաուժեղացնող ՌՆԹ պատվաստանյութի անվտանգություն և իմունոգենություն, որն արտահայտում է խարսխված RBD. Preprint medRxiv 1; Տեղադրվել է 2022.11.21.22281000 թվականի նոյեմբերի 22-ին: doi: https://doi.org/10.1101/2022.11.21.22281000
- Elliott T, et al. (2022) Ուժեղացված իմունային պատասխանները հետերոլոգ պատվաստումներից հետո ինքնաուժեղացող ՌՆԹ և mRNA COVID-19 պատվաստանյութերով: PLoS Pathog 18 (10): e1010885: Հրատարակված՝ 4 թվականի հոկտեմբերի 2022: DOI: https://doi.org/10.1371/journal.ppat.1010885
- Keikha, R., Hashemi-Shahri, SM & Jebali, A. Նոր բանավոր պատվաստանյութերի գնահատումը, որը հիմնված է ինքնահաստատվող ՌՆԹ-ի լիպիդային նանմասնիկների (saRNA LNPs), saRNA տրանսֆեկցված Lactobacillus plantarum LNP-ների և saRNA տրանսֆեկցված Lactobacillus plantarum SARS-CoV-ի վրա չեզոքացնելու համար: -2 տարբերակ ալֆա և դելտա: Sci Rep 11, 21308 (2021): Հրատարակված՝ 29 հոկտեմբերի 2021 թ. https://doi.org/10.1038/s41598-021-00830-5
- CDC 2022. Ինչպես են պատրաստվում գրիպի (գրիպի) պատվաստանյութերը: Հասանելի է առցանց՝ հասցեով https://www.cdc.gov/flu/prevent/how-fluvaccine-made.htm մուտք է գործել 18 թվականի դեկտեմբերի 2022-ին։
- Chang C., et al 2022. Ինքնահաստատվող mRNA բիցիստրոնիկ գրիպի պատվաստանյութերը բարձրացնում են խաչաձև ռեակտիվ իմունային պատասխանները մկների մոտ և կանխում վարակը լաստանավերի մոտ: Մոլեկուլային թերապիայի մեթոդներ և կլինիկական զարգացում: Հատոր 27, 8 Դեկտեմբեր 2022, Էջեր 195-205։ https://doi.org/10.1016/j.omtm.2022.09.013
***